Autor: prof. dr hab. inż. Iwona Skoczko
Wprowadzenie
Ultra czysta woda (UCW) stanowi fundament bezpieczeństwa mikrobiologicznego w nowoczesnych szpitalach i innych jednostkach medycznych. Jakość UCW oceniana jest najczęściej na wyjściu z systemu uzdatniania, zgodnie z obowiązującymi normami mikrobiologicznymi i chemicznymi. Takie podejście, choć technicznie poprawne, pomija jednak krytyczny aspekt bezpieczeństwa – zachowanie jakości wody w miejscu jej rzeczywistego użycia klinicznego, czyli w instalacjach końcowych (point-of-use).
Coraz więcej danych wskazuje, że instalacje końcowe UCW mogą stanowić istotne, a często niedoszacowane źródło biofilmów mikrobiologicznych, nawet w systemach spełniających rygorystyczne wymagania normatywne. Paradoksalnie, właściwości UCW, które czynią ją bezpieczną dla pacjenta, sprzyjają jednocześnie kolonizacji powierzchni instalacyjnych przez mikroorganizmy środowiskowe. Celem niniejszego artykułu przeglądowego jest kompleksowa analiza mechanizmów powstawania biofilmów w instalacjach point-of-use UCW, ich znaczenia klinicznego oraz luk projektowych i organizacyjnych, które sprzyjają temu zjawisku.
Instalacje końcowe (point-of-use) jako krytyczny punkt ryzyka w systemach ultra czystej wody
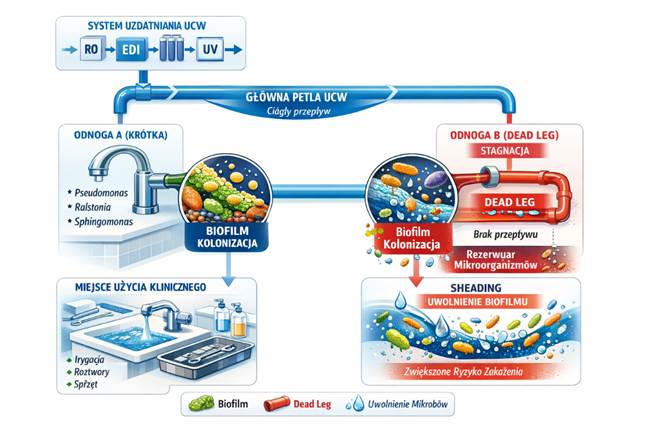
Rysunek 1. Ryzyko biofilmu w systemach UCW
Systemy ultra czystej wody w jednostkach medycznych projektowane są najczęściej w oparciu o koncepcję centralnego uzdatniania i dystrybucji wody w pętli zamkniętej, zapewniającej stabilne parametry fizykochemiczne na wyjściu ze stacji uzdatniania. W tym modelu główny nacisk kładzie się na skuteczność procesów technologicznych, takich jak odwrócona osmoza, dejonizacja, ultrafiltracja czy dezynfekcja promieniowaniem UV. Takie podejście, choć konieczne, okazuje się niewystarczające z punktu widzenia bezpieczeństwa klinicznego, jeżeli nie uwzględnia się specyfiki instalacji końcowych, czyli tzw. point-of-use (Prest et al., 2016; Petzold et al., 2017). Instalacje point-of-use obejmują wszystkie elementy systemu wodnego zlokalizowane pomiędzy główną pętlą dystrybucyjną UCW a miejscem jej faktycznego wykorzystania klinicznego. Są to m.in. wylewki, zawory poboru, perlatory, krótkie odcinki przyłączy, elastyczne przewody oraz urządzenia podłączane okresowo. W odróżnieniu od pętli głównej, instalacje te charakteryzują się przerywanym charakterem przepływu, zmiennością warunków hydraulicznych oraz występowaniem stagnacji wody. Czynniki te powodują, że strefa point-of-use stanowi najsłabsze ogniwo systemu UCW z punktu widzenia stabilności wody (Buse et al., 2012).
Szczególnie istotnym elementem instalacji końcowych są tzw. dead legs, czyli odcinki rurociągów lub przyłączy o ograniczonym lub zerowym przepływie. Dead legs powstają w wyniku nadmiarowego projektowania, pozostawiania rezerwowych punktów poboru lub okresowego wyłączania stanowisk z eksploatacji. Mogą one zaburzać warunki hydrauliczne i prowadzić do lokalnej degradacji jakości wody, niezależnie od parametrów mierzonych w pętli głównej (Bédard et al., 2015). Cechują się również zwiększoną interakcją wody z materiałami instalacyjnymi. Wysoka czystość chemiczna UCW sprzyja wymywaniu jonów, związków organicznych i dodatków technologicznych z powierzchni rur, uszczelek i armatury. Zjawisko to prowadzi do lokalnych zmian parametrów fizykochemicznych wody przedstawionych w tabeli 1, takich jak przewodność, pH czy zawartość biodostępnych związków węgla (Prest et al., 2016). W praktyce klinicznej instalacje końcowe pozostają często poza systematycznym nadzorem, zarówno na etapie projektowania, jak i eksploatacji. Odpowiedzialność za tę strefę bywa rozproszona pomiędzy zespoły techniczne i personel medyczny, a obowiązujące normy jakości wody koncentrują się głównie na parametrach mierzonych w punktach centralnych. W efekcie point-of-use stanowi obszar o najwyższym znaczeniu dla bezpieczeństwa pacjenta, a jednocześnie najsłabiej uregulowany i monitorowany element systemu UCW.
Ultra czysta woda jako środowisko selekcyjne: biofilm i mikroorganizmy kolonizujące systemy UCW
Ultra czysta woda, mimo spełniania rygorystycznych kryteriów chemicznych i mikrobiologicznych, nie jest środowiskiem jałowym, lecz specyficznym ekosystemem o silnie selektywnym charakterze. Jej niska przewodność, minimalna zawartość jonów, bardzo niski poziom węgla organicznego oraz brak dezynfektanta resztkowego tworzą warunki, w których przeżywają i dominują mikroorganizmy zdolne do funkcjonowania w środowiskach oligotroficznych.
Tabela 1. Charakterystyka parametrów ultra czystej wody (UCW) w systemach medycznych
| Parametr | Wyjście ze stacji uzdatniania UCW | Punkty końcowe (point-of-use) | Znaczenie mikrobiologiczne i kliniczne |
| Temperatura | typowo 15–25 °C (zależnie od instalacji i warunków zasilania) | 15–40 °C lokalnie; możliwe fluktuacje w zależności od otoczenia, przepływu i armatury | Wahania temperatury i epizodyczne „okno” 20–35 °C mogą sprzyjać kolonizacji i wzrostowi biofilmu |
| pH | 6,8–7,2 (bliskie obojętnemu) | zmienne; lokalne odchylenia (np. 6,5–8,0) | Odchylenia pH wpływają na adhezję, stabilność EPS oraz uwalnianie jonów z materiałów instalacyjnych |
| Przewodność elektryczna | ≤ 0,1–1,0 µS/cm (zwykle stabilna) | zmienna, często lokalnie podwyższona | Wzrost przewodności sugeruje wtórne „wzbogacanie” wody w jony (leaching, stagnacja, kontakt z armaturą) |
| TOC (całkowity węgiel organiczny) | bardzo niski (często <0,5 mg/L) | lokalnie podwyższony | Nawet niewielki wzrost TOC ułatwia inicjację biofilmu i wzrost bakterii oligotroficznych |
| AOC/BDOC (biodostępny C organiczny) | bardzo niski, często granica oznaczalności | wzrost lokalny w strefach stagnacji | Parametr krytyczny biologicznie – to „paliwo” dla biofilmu, nawet przy niskim TOC ogólnym |
| Tlen rozpuszczony (DO) | niski–umiarkowany (. ~0,5 -1 mg/L; zależnie od degazacji i technologii) | wyższy i zmienny (często 2–8 mg/L, możliwe wartości bliskie nasycenia) | Wyższy DO w point-of-use sprzyja bakteriom tlenowym; różnice DO tworzą mikrogradienty w biofilmie |
| Twardość ogólna | < 0,1 °dH (praktycznie „zero”) | lokalnie może wzrastać (śladowo) | Wzrost twardości zwykle wskazuje na wtórne uwalnianie Ca/Mg z armatury lub domieszkę wody gorszej jakości |
| Sole sodowe / sód (Na⁺) | < 1 mg/L | lokalnie wyższe | Wzrost Na⁺ może świadczyć o mieszaniu z wodą uzdatnioną niższej klasy lub migracji jonów w strefach stagnacji |
| Krzemiany (SiO₂ / silikaty) | < 0,1 mg/L | lokalnie mogą wzrastać | Krzemiany są markerem „przesiąkania” składu mineralnego i mogą sprzyjać osadom oraz stabilizacji powierzchni biofilmu |
| Ważne kationy | Ca²⁺, Mg²⁺ – śladowe; NH₄⁺ – śladowy/niewykrywalny | lokalne wzrosty (zwł. Ca²⁺/Mg²⁺); NH₄⁺ możliwy w epizodach | Ca²⁺/Mg²⁺ stabilizują EPS; NH₄⁺ to wysoko biodostępne źródło azotu (sprzyja wzrostowi) |
| Ważne aniony | PO₄³⁻, SO₄²⁻ – śladowe; HCO₃⁻ i NO₃⁻ – zwykle bardzo niskie | lokalne wzrosty (HCO₃⁻, NO₃⁻, PO₄³⁻) | PO₄³⁻ (fosfor) bywa czynnikiem limitującym; NO₃⁻/HCO₃⁻ wpływają na metabolizm i buforowanie pH |
| Mikrobiologia (bakterie hodowlane) | BRAK / 0 CFU (docelowo) | niestabilna; epizodyczne wzrosty | Kluczowy paradoks UCW: zgodność na wyjściu nie chroni przed kolonizacją point-of-use (biofilm) |
| Endotoksyny | niskie (docelowo minimalne) | zmienne; możliwe epizodyczne wzrosty | Endotoksyny mogą pojawiać się wtórnie w wyniku biofilmu Gram-ujemnego i zdarzeń „shedding” |
| Dezynfektant resztkowy | brak | brak | Brak „ochrony resztkowej” ułatwia wtórną kolonizację i stabilizację biofilmu |
| Przepływ | ciągły, projektowany na turbulentny | przerywany, często laminarny/stagnacyjny | Przerwy w przepływie i stagnacja są najsilniejszym czynnikiem ryzyka biofilmu |
| Ryzyko stagnacji / dead legs | minimalne (w dobrze zaprojektowanej pętli) | wysokie (odnogi, rzadkie punkty poboru, elastyczne przyłącza) | Najczęstsza lokalizacja biofilmu i rezerwuar uwalniania bakterii do strumienia wody |
Właściwości te sprawiają, że UCW sprzyja rozwojowi specyficznych strategii przetrwania mikroorganizmów, z których najważniejszą jest tworzenie biofilmu (Kulakov 2002). Biofilm stanowi dominującą formę bytowania mikroorganizmów w systemach wodnych, w tym w instalacjach UCW. Jest to zorganizowana struktura komórek mikrobiologicznych osadzonych na powierzchniach i otoczonych macierzą zewnątrzkomórkową, złożoną głównie z polisacharydów, białek i pozakomórkowego DNA. Taka organizacja zapewnia ochronę przed czynnikami środowiskowymi, stabilność mechaniczną oraz zwiększoną tolerancję na środki dezynfekcyjne i stresy fizykochemiczne (Flemming et al., 2016). W środowisku UCW biofilm pełni kluczową funkcję adaptacyjną. Brak łatwo dostępnych substancji odżywczych oraz brak dezynfekanta resztkowego powodują, że mikroorganizmy przechodzą z form planktonowych w formy związane z powierzchnią. W strukturze biofilmu możliwe jest efektywne wykorzystanie śladowych ilości biodostępnego węgla organicznego, jonów nieorganicznych oraz tlenu, co umożliwia długotrwałe przetrwanie kolonii nawet w warunkach ekstremalnie niskiego obciążenia substancjami pożywkowymi (Prest et al., 2016).
Mikroorganizmy kolonizujące systemy UCW należą głównie do Gram-ujemnych bakterii środowiskowych o wysokim potencjale adaptacyjnym. Najczęściej identyfikowane są przedstawiciele rodzajów Pseudomonas, Ralstonia, Sphingomonas, Burkholderia oraz Acinetobacter. Drobnoustroje te charakteryzują się zdolnością do wzrostu w warunkach oligotroficznych, wysoką tolerancją na stres osmotyczny oraz predyspozycją do tworzenia trwałych struktur biofilmowych (Whiley et al., 2015).
Tabela 2. Mikroorganizmy w systemach ultra czystej wody (UCW) w jednostkach medycznych
| Mikroorganizmy kolonizujące UCW | Warunki sprzyjające rozwojowi w systemach UCW |
| Pseudomonas aeruginosa | Niski przepływ, obecność biofilmu, zmienna temperatura |
| Ralstonia pickettii | Bardzo niska zawartość składników odżywczych, brak dezynfektanta resztkowego |
| Sphingomonas paucimobilis | Wysoka czystość chemiczna wody, powierzchnie polimerowe |
| Burkholderia cepacia complex | Stagnacja, obecność elastomerów i uszczelek |
| Acinetobacter spp. | Biofilm, wilgotne środowisko, niska konkurencja mikrobiologiczna |
| Stenotrophomonas maltophilia | Niski TOC, brak chloru, okresowe użytkowanie instalacji |
| Mycobacterium non-tuberculous (NTM) | Ciepła woda, biofilm, odporność na dezynfekcję |
| Legionella spp. | Dead legs, stagnacja, temperatury pośrednie |
| Bakterie Gram-ujemne oligotroficzne | UCW o bardzo niskiej przewodności i jonowości |
| Mikroorganizmy środowiskowe MDR | Presja selekcyjna, biofilm jako rezerwuar genów oporności |
Istotnym aspektem mikrobiologii UCW jest zdolność biofilmów do pełnienia funkcji rezerwuarów genów oporności na antybiotyki oraz determinant tolerancji na środki dezynfekcyjne. W obrębie biofilmu zachodzi intensywna wymiana materiału genetycznego pomiędzy mikroorganizmami, co sprzyja utrwalaniu cech adaptacyjnych i zwiększa ich zdolność przetrwania w środowisku szpitalnym (Bar-On, 2019). Dodatkowo biofilm może stanowić źródło okresowego uwalniania komórek bakteryjnych do strumienia wody, co prowadzi do nieprzewidywalnych epizodów ekspozycji klinicznej (Bédard et al., 2015). W świetle powyższych danych mikrobiologia UCW powinna być analizowana nie wyłącznie w kategoriach zgodności normatywnej, lecz jako dynamiczny proces biologiczny zachodzący w całym systemie wodnym.
Konsekwencje kliniczne i implikacje dla kontroli zakażeń
Obecność mikrobiologicznych zagrożeń związanych z systemami ultra czystej wody w jednostkach medycznych ma bezpośrednie i pośrednie konsekwencje kliniczne, które w wielu przypadkach pozostają niedoszacowane lub błędnie przypisywane innym źródłom zakażeń. W przeciwieństwie do klasycznych rezerwuarów patogenów szpitalnych, takich jak ręce personelu czy powierzchnie kontaktowe, zagrożenia wodnopochodne charakteryzują się trudną wykrywalnością, nieregularnością występowania oraz ograniczoną korelacją z rutynowymi wynikami monitoringu mikrobiologicznego wody (Petzold et al., 2017). Jednym z najistotniejszych klinicznie aspektów ekspozycji na mikroorganizmy związane z systemami UCW są zakażenia o charakterze sporadycznym lub klastrowym, które nie wpisują się w typowe wzorce epidemiologiczne. Okresowe uwalnianie mikroorganizmów z instalacji końcowych może prowadzić do nagłych epizodów kontaminacji roztworów, płynów irygacyjnych lub sprzętu medycznego, skutkując zakażeniami miejsca operowanego, zakażeniami krwiopochodnymi lub zakażeniami układu oddechowego, szczególnie u pacjentów o obniżonej odporności (Percival et al., 2015). Szczególnie wysokie ryzyko kliniczne dotyczy oddziałów intensywnej terapii, jednostek transplantacyjnych, stacji dializ oraz bloków operacyjnych. W tych środowiskach nawet niskopatogenne mikroorganizmy środowiskowe mogą powodować ciężkie zakażenia, w tym bakteriemie, zapalenia płuc czy zakażenia ran pooperacyjnych. Co istotne, patogeny wodnopochodne często wykazują podwyższoną tolerancję na antybiotyki i środki dezynfekcyjne, co dodatkowo komplikuje proces leczenia i zwiększa ryzyko niepowodzeń terapeutycznych (Whiley et al., 2015).
Z perspektywy kontroli zakażeń problem UCW ujawnia fundamentalną lukę pomiędzy formalną zgodnością normatywną a rzeczywistym bezpieczeństwem pacjenta. Standardowe programy nadzoru epidemiologicznego rzadko uwzględniają instalacje wodne jako potencjalne źródło zakażeń, a dochodzenia epidemiologiczne często koncentrują się na bezpośrednich czynnikach klinicznych. W rezultacie zakażenia związane z wodą bywają klasyfikowane jako idiopatyczne lub przypisywane transmisji kontaktowej, co opóźnia identyfikację rzeczywistego źródła problemu (Bédard et al., 2015). Implikacje dla systemów kontroli zakażeń są wielowymiarowe. Po pierwsze, zarządzanie ryzykiem wodnopochodnym wymaga rozszerzenia klasycznych strategii kontroli zakażeń o elementy inżynierskie i środowiskowe. Obejmuje to ścisłą współpracę zespołów kontroli zakażeń, inżynierii klinicznej oraz utrzymania ruchu, co w wielu placówkach nie jest jeszcze standardem organizacyjnym. Po drugie, konieczne jest odejście od wyłącznie reaktywnego modelu postępowania, opartego na analizie ognisk zakażeń, na rzecz podejścia proaktywnego, uwzględniającego ocenę ryzyka instalacji wodnych jeszcze przed wystąpieniem incydentów klinicznych (Petzold et al., 2017). Istotnym wyzwaniem jest również ograniczona przydatność rutynowych badań mikrobiologicznych w kontekście UCW. Klasyczne metody hodowlane, stosowane w nadzorze sanitarno-epidemiologicznym, nie odzwierciedlają rzeczywistego ryzyka klinicznego wynikającego z obecności mikroorganizmów związanych z powierzchniami instalacyjnymi. W konsekwencji systemy kontroli zakażeń, oparte wyłącznie na wynikach badań próbek wody, mogą generować fałszywe poczucie bezpieczeństwa (Percival et al., 2014).
Z punktu widzenia praktyki klinicznej istotne jest uwzględnienie ryzyka wodnopochodnego w procedurach wysokiego ryzyka, takich jak przygotowywanie roztworów jałowych, irygacja tkanek, obsługa sprzętu do terapii oddechowej czy procedury wykonywane u pacjentów immunoniekompetentnych. W tych obszarach nawet krótkotrwała ekspozycja na mikroorganizmy środowiskowe może prowadzić do poważnych konsekwencji zdrowotnych. Coraz więcej autorów podkreśla, że skuteczna kontrola zakażeń w nowoczesnych szpitalach nie może pomijać systemów wodnych jako integralnego elementu środowiska klinicznego (Flemming et al., 2016). Konsekwencje kliniczne związane z UCW mają również wymiar ekonomiczny i organizacyjny. Zakażenia wodnopochodne prowadzą do wydłużenia hospitalizacji, wzrostu kosztów leczenia, konieczności stosowania antybiotyków o szerokim spektrum oraz obciążenia systemów raportowania zdarzeń niepożądanych. W dłuższej perspektywie brak systemowego podejścia do zarządzania UCW może podważać zaufanie do procedur kontroli zakażeń i negatywnie wpływać na jakość opieki zdrowotnej.
Strategie projektowe i eksploatacyjne ograniczające ryzyko związane z ultra czystą wodą
Skuteczne ograniczenie ryzyka klinicznego związanego z systemami UCW wymaga odejścia od podejścia skoncentrowanego wyłącznie na jakości wody na wyjściu ze stacji uzdatniania i przyjęcia perspektywy systemowej, obejmującej projektowanie, eksploatację oraz długoterminowe zarządzanie całym układem, ze szczególnym uwzględnieniem instalacji końcowych. W literaturze coraz częściej podkreśla się, że UCW powinna być traktowana jako element infrastruktury krytycznej szpitala, a nie wyłącznie jako medium technologiczne (Petzold et al., 2017).
Na etapie projektowym duże znaczenie ma hydrauliczna i funkcjonalna optymalizacja systemu dystrybucji UCW. Projekt pętli dystrybucyjnej powinien zapewniać ciągły, możliwie turbulentny przepływ wody, minimalizując strefy stagnacji i ograniczając liczbę odgałęzień. Szczególną uwagę należy zwrócić na eliminację dead legs już na etapie koncepcji instalacji i rezygnację z rezerwowych przyłączy bez jasno określonej funkcji. Jeżeli są ważne w projekcie, powinny być uwzględnione w sposób umożliwiający regularne płukanie lub okresową dezynfekcję (Bédard et al., 2015).
Istotnym elementem strategii projektowej jest również dobór materiałów instalacyjnych przedstawionych w tabeli 3. Materiały mające kontakt z UCW powinny charakteryzować się niską podatnością na adhezję mikroorganizmów, wysoką odpornością chemiczną oraz minimalnym potencjałem wymywania jonów i związków organicznych. W praktyce oznacza to preferowanie stali nierdzewnej o odpowiedniej jakości powierzchni, ograniczanie stosowania elastomerów i tworzyw sztucznych w strefach point-of-use oraz unikanie materiałów o porowatej strukturze powierzchni. Dobór materiałów powinien uwzględniać nie tylko zgodność z normami technicznymi, ale również ich zachowanie w długotrwałym kontakcie z wodą o bardzo niskiej mineralizacji (Prest et al., 2016).
Tabela 3. Materiały stosowane w instalacjach wodociągowych jednostek medycznych
| Materiał instalacyjny | Zastosowanie w szpitalach | Podatność na korozję w UCW | Uwalnianie jonów / związków do wody | Podatność na adhezję mikroorganizmów | Komentarz kliniczno-techniczny |
| Stal nierdzewna AISI 316L (polerowana) | Pętle UCW, farmacja, dializa | Niska (przy prawidłowej pasywacji) | Bardzo niska (Fe, Cr, Ni – śladowe) | Niska | Złoty standard dla UCW; gładka powierzchnia ogranicza inicjację biofilmu |
| Stal nierdzewna AISI 304 | Instalacje pomocnicze | Średnia | Możliwe uwalnianie Fe, Ni | Średnia | Mniejsza odporność korozyjna; niezalecana do krytycznych punktów UCW |
| Miedź (Cu) | Woda użytkowa, instalacje tradycyjne | Średnia w UCW (agresywność wody) | Uwalnianie Cu²⁺ (istotne) | Niska (działanie bakteriostatyczne) | Silne właściwości antybakteryjne; niekompatybilna z UCW z powodu korozji i jonów |
| Mosiądz (Cu–Zn) | Armatura, zawory | Średnia | Cu²⁺, Zn²⁺ (śladowo Pb w starszych stopach) | Niska–średnia (działanie bakteriostatyczne) | Antybakteryjny, lecz ryzyko wymywania metali; niezalecany do point-of-use UCW |
| PVC / PVC-U | Instalacje wtórne | Brak korozji | Migracja związków organicznych | Wysoka | Brak korozji ≠ bezpieczeństwo mikrobiologiczne; wysoki potencjał biofilmu |
| PEX | Przyłącza, modernizacje | Brak | Migracja BDOC | Wysoka | Szczególnie problematyczny w UCW (biofilm + stagnacja) |
| PP-R | Woda technologiczna | Brak | Niska–umiarkowana migracja organiki | Średnia–wysoka | Lepszy niż PEX, nadal biologicznie aktywny |
| PVDF | Systemy wysokiej czystości | Brak | Bardzo niska | Niska | Bardzo dobra kompatybilność z UCW; wysoki koszt |
| PTFE (teflon) | Uszczelnienia | Brak | Brak | Niska | Chemicznie obojętny, biologicznie korzystny |
| EPDM / elastomery | Uszczelki, zawory | Brak | Migracja dodatków | Wysoka | Krytyczny punkt inicjacji biofilmu w point-of-use |
| Silikon | Przewody elastyczne | Brak | Migracja niskocząsteczkowa | Bardzo wysoka | Jeden z głównych rezerwuarów biofilmu |
| Guma naturalna | Starsze instalacje | Brak | Wysoka migracja | Bardzo wysoka | Niezalecana w środowisku UCW |
Warto zwrócić uwagę na działanie bakteriostatyczne miedzi i jej stopów, które jest dobrze udokumentowane i wynika z uwalniania jonów Cu²⁺, które destabilizują błony komórkowe bakterii, indukują stres oksydacyjny i zaburzają funkcje enzymatyczne. W klasycznych instalacjach wody użytkowej właściwość ta może ograniczać kolonizację mikrobiologiczną. Jednak w systemach ultra czystej wody agresywność chemiczna medium prowadzi do nadmiernego uwalniania jonów metali, co jest nieakceptowalne z punktu widzenia jakości UCW i bezpieczeństwa klinicznego. W konsekwencji miedź i mosiądz, mimo korzystnych właściwości mikrobiologicznych, nie są materiałami odpowiednimi dla systemów UCW, zwłaszcza w strefach point-of-use.
Na etapie eksploatacyjnym kluczową rolę odgrywa zarządzanie przepływem i użytkowaniem systemu UCW. Regularne użytkowanie punktów poboru, planowe płukanie instalacji końcowych oraz unikanie długotrwałej stagnacji stanowią podstawowe, lecz często niedoceniane elementy ograniczania ryzyka. W praktyce oznacza to konieczność opracowania harmonogramów płukania dla rzadko używanych punktów poboru oraz ścisłego monitorowania rzeczywistego wykorzystania instalacji, a nie jedynie jej parametrów projektowych (Percival et al., 2014).
Dezynfekcja systemów UCW stanowi kolejny filar strategii eksploatacyjnej. W przeciwieństwie do klasycznych instalacji wody pitnej, systemy UCW pozbawione są dezynfektanta resztkowego, co wymaga stosowania dezynfekcji okresowej lub punktowej. Dobór metody dezynfekcji powinien uwzględniać specyfikę instalacji, kompatybilność materiałową oraz potencjalny wpływ na jakość wody. Coraz częściej zaleca się łączenie metod fizycznych i chemicznych, takich jak dezynfekcja termiczna, promieniowanie UV czy środki utleniające stosowane w kontrolowanych cyklach, przy jednoczesnym monitorowaniu skuteczności zabiegów w punktach końcowych (Flemming et al., 2016).
Integralnym elementem strategii ograniczania ryzyka UCW jest również rozwój systemów monitoringu, wykraczających poza klasyczne badania mikrobiologiczne próbek wody. Nowoczesne podejścia obejmują monitorowanie parametrów fizykochemicznych w czasie rzeczywistym, analizę trendów jakościowych oraz okresowe badania powierzchni instalacji końcowych. Tego rodzaju monitoring pozwala na wczesne wykrywanie zmian w funkcjonowaniu systemu, zanim przełożą się one na konsekwencje kliniczne (Prest et al., 2016).
Kierunki badań i rekomendacje rozwoju systemów ultra czystej wody (gap analysis)
Pomimo rosnącej świadomości znaczenia ultra czystej wody w środowisku klinicznym, aktualny stan wiedzy i praktyki wskazuje na istnienie licznych luk badawczych oraz niedostosowanie obowiązujących standardów do rzeczywistych zagrożeń występujących w jednostkach medycznych. Najistotniejszą zidentyfikowaną luką jest rozbieżność pomiędzy normatywną oceną jakości UCW a rzeczywistym bezpieczeństwem mikrobiologicznym w punktach końcowych instalacji. Obowiązujące wytyczne koncentrują się niemal wyłącznie na parametrach wody mierzonej na wyjściu ze stacji uzdatniania lub w głównej pętli dystrybucyjnej, pomijając dynamikę procesów zachodzących w instalacjach point-of-use, które – jak wykazano w poprzednich sekcjach – stanowią kluczowy obszar ryzyka klinicznego.
Jednym z podstawowych kierunków przyszłych badań powinna być systematyczna ocena relacji pomiędzy parametrami fizykochemicznymi UCW a inicjacją i stabilnością kolonizacji mikrobiologicznej w instalacjach końcowych. Dotychczasowe prace analizują te zagadnienia fragmentarycznie, często w oderwaniu od rzeczywistych warunków eksploatacyjnych szpitali. Konieczne są badania prospektywne prowadzone w warunkach klinicznych, uwzględniające zmienność użytkowania, sezonowość oraz różnice pomiędzy oddziałami o odmiennym profilu ryzyka. Szczególną uwagę należy poświęcić parametrom biologicznie istotnym, takim jak biodostępny węgiel organiczny, lokalne gradienty tlenu, obecność śladowych jonów oraz interakcje UCW z materiałami instalacyjnymi. Kolejną istotną luką jest ograniczona dostępność narzędzi monitorowania biofilmów dostosowanych do środowiska szpitalnego. Aktualnie stosowane metody opierają się głównie na punktowych badaniach próbek wody, które nie odzwierciedlają obecności mikroorganizmów związanych z powierzchniami. Kierunkiem rozwoju powinny być metody monitoringu powierzchniowego i molekularnego, umożliwiające wczesne wykrywanie kolonizacji instalacji końcowych oraz ocenę skuteczności działań prewencyjnych. Rozwój czujników on-line, systemów predykcyjnych oraz analiz trendów jakościowych może znacząco zwiększyć zdolność do proaktywnego zarządzania ryzykiem UCW.
Z perspektywy kontroli zakażeń szczególną luką pozostaje brak integracji zarządzania UCW z systemami nadzoru epidemiologicznego. W większości placówek instalacje wodne nie są rutynowo uwzględniane w analizach przyczyn zakażeń, a zespoły kontroli zakażeń mają ograniczony dostęp do danych technicznych dotyczących eksploatacji systemów UCW. Kierunkiem rozwoju powinno być tworzenie interdyscyplinarnych modeli oceny ryzyka, łączących dane kliniczne, mikrobiologiczne i inżynierskie w ramach jednego systemu decyzyjnego. Rekomendacje rozwojowe obejmują również konieczność rewizji obowiązujących norm i wytycznych dotyczących UCW w kontekście środowiska szpitalnego. Obecne regulacje, w dużej mierze oparte na standardach dializacyjnych i farmaceutycznych, nie uwzględniają specyfiki instalacji point-of-use oraz różnic w profilu ryzyka pomiędzy oddziałami. W przyszłości zasadne wydaje się wprowadzenie podejścia opartego na ocenie ryzyka (risk-based water quality management), w którym wymagania jakościowe i zakres monitoringu byłyby dostosowane do rodzaju procedur klinicznych i populacji pacjentów. Wreszcie, istotnym, choć często pomijanym kierunkiem rozwoju jest aspekt organizacyjny i edukacyjny. Skuteczne zarządzanie UCW wymaga nie tylko rozwiązań technicznych, ale również odpowiedniego przygotowania personelu oraz jasno zdefiniowanej odpowiedzialności za systemy wodne. Włączenie zagadnień związanych z UCW do programów szkoleń z zakresu kontroli zakażeń oraz inżynierii klinicznej może znacząco poprawić zdolność placówek do identyfikowania i ograniczania ryzyka wodnopochodnego.
Podsumowanie i wnioski
Przedstawiona analiza jednoznacznie wskazuje, że systemy ultra czystej wody w jednostkach medycznych należy postrzegać jako dynamiczne układy środowiskowe, a nie wyłącznie jako element infrastruktury technicznej spełniającej określone normy jakościowe. Pomimo wysokiej skuteczności procesów uzdatniania, formalna zgodność parametrów UCW na wyjściu ze stacji nie gwarantuje bezpieczeństwa mikrobiologicznego w miejscu jej rzeczywistego wykorzystania klinicznego. Kluczowym obszarem ryzyka pozostają instalacje końcowe (point-of-use), w których specyfika hydrauliczna, materiałowa i eksploatacyjna sprzyja wtórnym zmianom jakości wody.
- Czynniki takie jak stagnacja przepływu, obecność dead legs, zmienność temperatury oraz interakcje UCW z materiałami instalacyjnymi prowadzą do lokalnej degradacji parametrów fizykochemicznych wody.
- Z kolei perspektywa mikrobiologiczna ujawnia, że ultra czysta woda stanowi środowisko selekcyjne sprzyjające przetrwaniu mikroorganizmów oligotroficznych, dla których tworzenie biofilmu jest podstawową strategią adaptacyjną.
- Konsekwencje kliniczne mają szczególne znaczenie w oddziałach wysokiego ryzyka, jak bloki operacyjne, oddziały intensywnej terapii, jednostki transplantacyjne czy stacje dializ. Zakażenia często mają charakter sporadyczny, trudny do jednoznacznego przypisania i mogą być błędnie klasyfikowane w systemach nadzoru epidemiologicznego.
- Przegląd dostępnych strategii projektowych i eksploatacyjnych wskazuje, że skuteczne ograniczanie ryzyka związanego z UCW wymaga podejścia systemowego, obejmującego cały cykl życia instalacji – od etapu projektowania, poprzez codzienną eksploatację, aż po długoterminowe monitorowanie i doskonalenie procedur.
- Kluczowe znaczenie ma eliminacja stref stagnacji, świadomy dobór materiałów instalacyjnych, zarządzanie przepływem oraz wdrażanie metod dezynfekcji i monitoringu dostosowanych do specyfiki instalacji końcowych.
- Analiza luk badawczych wskazuje na potrzebę rewizji obowiązujących norm i wytycznych dotyczących UCW w środowisku szpitalnym. Należy zmierzać w kierunku modeli zarządzania opartych na ocenie ryzyka, uwzględniających różnice w profilu klinicznym oddziałów oraz rzeczywiste warunki eksploatacyjne instalacji point-of-use.
LITERATURA
- Bédard, Emilie, et al. „Impact of stagnation and sampling volume on water microbial quality monitoring in large buildings.” PloS one 13.6 (2018): e0199429.
- Buse, Helen Y., et al. „Effect of temperature and colonization of Legionella pneumophila and Vermamoeba vermiformis on bacterial community composition of copper drinking water biofilms.” Microbial Biotechnology 10.4 (2017): 773-788.
- Ashbolt, Nicholas J. „Environmental (saprozoic) pathogens of engineered water systems: understanding their ecology for risk assessment and management.” Pathogens 4.2 (2015): 390-405.
- Exner M.
Petzold, Markus, et al. „Rapid genotyping of Legionella pneumophila serogroup 1 strains by a novel DNA microarray-based assay during the outbreak investigation in Warstein, Germany 2013.” International journal of hygiene and environmental health 220.4 (2017): 673-678. - Flemming, Hans-Curt, et al. „Biofilms: an emergent form of bacterial life.” Nature Reviews Microbiology 14.9 (2016): 563-575.
- Bar-On, Yinon M., and Ron Milo. „Towards a quantitative view of the global ubiquity of biofilms.” Nature Reviews Microbiology 17.4 (2019): 199-200.
- Percival, Steven L., et al. „Healthcare-associated infections, medical devices and biofilms: risk, tolerance and control.” Journal of medical microbiology 64.4 (2015): 323-334.
- Prest, E. I., et al. „A systematic approach for the assessment of bacterial growth-controlling factors linked to biological stability of drinking water in distribution systems.” Water Science and Technology: Water Supply 16.4 (2016): 865-880.
- Whiley, Harriet. Legionella spp., L. pneumophila and Mycobacterium avium complex (MAC) in potable and reuse water distribution pipelines. Diss. Flinders University, School of the Environment., 2015.
- Kulakov, Leonid A., et al. „Analysis of bacteria contaminating ultrapure water in industrial systems.” Applied and environmental microbiology 68.4 (2002): 1548-1555.

